Молекулярно-кинетическая теория
|
Экспериментальные газовые законы | ||
|
Изопроцессы. Законы Бойля-Мариотта, Гей-Люссака, Шарля. | ||
|
| Всякое изменение состояния газа называется термодинамическим процессом.
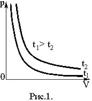
Простейшими процессами в идеальном газе являются изопроцессы. Это процессы, при которых масса газа и один из его параметров состояния (температура, давление или объем) остаются постоянными. Изопроцесс, протекающий при постоянной температуре, называется изотермическим. Экспериментально Р. Бойлем и Э. Мариоттом было установлено, что при постоянной температуре произведение давления газа на объем для данной массы газа есть величина постоянная (закон Бойля–Мариотта):
Графически этот закон в координатах РV изображается линией, называемой изотермой (рис.1). | |
|
|
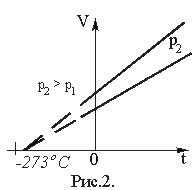
Изопроцесс, протекающий в идеальном газе, в ходе которого давление остается постоянным, называется изобарным. Зависимость объема газа от его температуры при постоянном давлении была установлена Л. Гей-Люссаком, который показал, что объем газа данной массы при постоянном давлении возрастает линейно с увеличением температуры (закон Гей-Люссака): V = V0·(1 + ·t), (17) где V – объем газа при температуре t, °С; V0 – его объем при 0°С. Величина V = V0·(1 + Графически зависимость объема от температуры изображается прямой линией – изобарой (рис. 2). При очень низких температурах (близких к – 273°С) закон Гей–Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром. | |
|
|
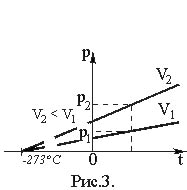
Изопроцесс, протекающий в газе, при котором объем остается постоянным, называется изохорным. Исследования зависимости давления данной массы газа от температуры при неизменном объеме были впервые проведены французским физиком Шарлем. Им было установлено, что давление газа данной массы при постоянном объеме возрастает линейно с увеличением температуры (закон Шарля): P = P0(1+ Здесь P – давление газа при температуре t, °С; P0 – его давление при 0 °С. Величина P = P0(1 + Графическая зависимость давления от температуры изображается прямой линией – изохорой (Рис. 3). | |
|
Абсолютная шкала температур. Если изохору продолжить в область отрицательных температур, то в точке пересечения с осью абсцисс имеем P = P0(1 + Отсюда температура, при которой давление идеального газа обращается в нуль, t = –273°С (точнее,–273,16°С). Эта температура выбрана в качестве начала отсчета термодинамической шкалы температур, которая была предложена английским ученым Кельвиным. Эта температура называется нулем Кельвина (или абсолютным нулем). Температура, отсчитанная по термодинамической шкале температур, обозначается Т. Ее называют термодинамической температурой. Так как точка плавления льда при нормальном атмосферном давлении, принятая за 0°С, равна 273,16 К–1, то Т = 273,16 + t. (22) Уравнение Клайперона. Получим другую форму уравнений, описывающих изобарный и изохорный процессы, заменив в уравнениях (18) и (20) температуру, отсчитанную по шкале Цельсия, термодинамической температурой: V = V0(1 + Обозначив объемы газа при температурах Т1 и Т2, как V1 и V2, запишем V1 = V0 Разделив почленно эти равенства, получим закон Гей - Люссака в виде V1/V2 = Т1/Т2 или
Аналогично получим новую форму закона Шарля :
Законы Шарля и Гей-Люссака можно объединить в один общий закон, связывающий параметры P, V и T при неизменной массе газа. Действительно, предположим, что начальное состояние газа при m = const характеризуется параметрами V1, Р1, Т1, а конечное – соответственно V2, Р2, Т2. Пусть переход из начального состояния в конечное состояние происходит с помощью двух процессов: изотермического и изобарического. В ходе первого процесса изменим давление с Р1 на Р2. Объем, который займет газ после этого перехода, обозначим V, тогда по закону Бойля–Мариотта, Р1V1 = Р2V, откуда
На втором этапе уменьшим температуру с Т1 до Т2, при этом объем изменится от значения V до V2; следовательно по закону Шарля
В уравнениях (25) и (26) равны левые части; следовательно, равны и правые, тогда
т. е. можно записать, что
Выражение (28) называют уравнением Клапейрона или объединённым газовым законом. Уравнение состояния идеального газа – уравнение Менделеева-Клапейрона. Значение входящей в уравнение (28) константы, которая обозначается как R, для одного моля любого газа одинаково, поэтому эта константа получила название универсальной газовой постоянной. Найдем числовое значение R в СИ, для чего учтем, что, как следует из закона Авогадро, один моль любого газа при одинаковом давлении и одинаковой температуре занимает один и тот же объем. В частности при Т0 = 273K и давлении Р0 = 105 Па объем одного моля газа равен V0 = 22,4·10–³ м³. Тогда R = Уравнение (28) для одного моля газа можно записать в виде
Из уравнения (29) легко получить уравнение для любой массы газа. Газ массой m займет объем V = V0(m/M), где М – масса 1 моль, m/M – число молей газа. Умножив обе части уравнения (29) на m/M, получим Так как
Уравнение (30) называется уравнением Менделеева – Клапейрона и является основным уравнением, связывающим параметры газа в состоянии теплового равновесия. Поэтому его называют уравнением состояния идеального газа. | ||
|
Температура - мера средней кинетической энергии | ||
|
Сравнивая уравнение состояния идеального газа и основное уравнение кинетической теории газов, записанные для одного моля (для этого число молекул N возьмём равным числу Авогадро NА), найдём среднюю кинетическую энергию одной молекулы:
Откуда
Средняя кинетическая энергия поступательного движения молекулы не зависит от её природы и пропорциональна абсолютной температуре газа T. Отсюда следует, что абсолютная температура является мерой средней кинетической энергии молекул. Величина R/NА = k в уравнении (31) получила название постоянной Больцмана и представляет собой газовую постоянную, отнесенную к одной молекуле: k = 1,38·10-23 Дж/К-23. Так как
Подставляя значение средней кинетической энергии поступательного движения молекул (31) в основное уравнение молекулярно–кинетической теории газов, получим другую форму уравнения состояния идеального газа: P = n0kT. (33) Давление газа пропорционально произведению числа молекул в единице объема на его термодинамическую температуру.
На рис. приведена схема опыта Штерна для определения скорости молекул газа. В нагревателе с поверхности проволоки, раскаленной электрическим током, испаряются атомы серебра. Попадая из нагревателя через отверстие в вакуумную камеру, молекулы пара с помощью системы щелей формируются в узкий пучок, направленный в сторону двух дисков, вращающихся с угловой скоростью w .Диски используются для сортировки молекул по скоростям. Угол между прорезями в дисках q. Расстояние между дисками X в процессе эксперимента не изменяется. Для того, чтобы молекула пара попала на приемник детектора частиц, она должна пройти через прорези в дисках. Для этого время прохождения молекулы, движущейся со скоростью V между дисками, должно быть равно времени поворота прорези второго диска на угол q. Поэтому V=w· X/ q | ||

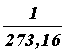 ·t) = V0(
·t) = V0(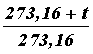 ) = V0
) = V0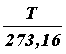
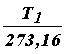 , V2 = V0
, V2 = V0 .
.
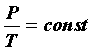 (24)
(24)
 , или
, или
 , (27)
, (27)
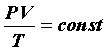 . (28)
. (28)
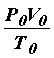 = 8,31 Дж/(моль· К).
= 8,31 Дж/(моль· К).
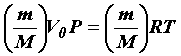 .
.
 , то окончательно получаем
, то окончательно получаем
 . (30)
. (30)
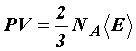 и
и  . (31)
. (31)
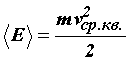 =
=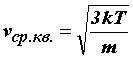 . (32)
. (32)
