Влияние вращательного и поступательного движения молекул на теплоёмкость многоатомных газов
![]()
![]()
![]()
Благодаря большой величине моментов инерции многоатомных молекул (и соответственно малости их вращательных квантов) их вращение можно всегда рассматривать классически[1]. Многоатомӯная молекула обладает тремя вращательными степенями свободы и тремя в общем случае различными главными моментами инерӯции I1, I2, I3; поэтому ее кинетическая энергия вращения есть
![]()
где x, h, z — координаты вращающейся системы, оси которой соӯвпадают с главными осями инерции молекулы, (оставляем пока в стороне особый случай молекул, составленных из атомов, расӯположенных на одной прямой). Это выражение должно быть подӯставлено в статистический интеграл
 (2.1)
(2.1)
где
![]()
а штрих у интеграла означает, что интегрирование должно производиться лишь по тем ориентациям молекулы, котоӯрые физически отличны друг от друга.
Если молекула обладает какими-либо осями симметрии, то поӯвороты вокруг этих осей совмещают молекулу саму с собой и своӯдятся к перестановке одинаковых атомов. Ясно, что число физиӯчески неразличимых ориентации молекулы равно числу допускаеӯмых ею различных поворотов вокруг осей симметрии (включая тождественное преобразование—поворот на 360°). Обозначив это число посредством s [2] , можно производить интегрирование в (2.1) просто по всем ориентациям, одновременно разделив все выраӯжение на s. В произведении djxdjhdjz (трех бесконечно малых углов повоӯрота) можно рассматривать djx, djh, как элемент dsz телесного угла для направлений оси z.
Интегрирование по dsz производится неӯзависимо от интегрирования по поворотам djz вокруг самой оси z и дает 4p. После этого интегрирование по djz дает еще 2p.
Интегрируя также и по dMxdMhdMz (в пределах от -¥ до +¥), найдем в результате
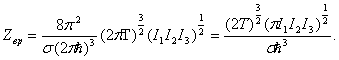
Отсюда свободная энергия

Таким образом, для вращательной теплоемкости имеем в соотӯветствии с (1.3)
![]()
а химическая постоянная

Если все атомы в молекуле расположены на одной прямой (линейная молекула), то она обладает, как и двухатомная молеӯкула, всего двумя вращательными степенями свободы и одним моментом инерции /. Вращательные теплоемкость и химическая постоянная равны, как и у двухатомного газа,
![]()
![]()
где s=1 для несимметричной молекулы (например, NNO) и s=2 для молекулы, симметричной относительно своей середины (наӯпример, ОСО).
Колебания молекул.
Колебательная часть термодинамических величин газа станоӯвится существенной при значительно более высоких температуӯрах, чем вращательная, потому что интервалы колебательной структуры термов велики по сравнению с интервалами вращаӯтельной структуры.
Мы будем считать, однако, температуру большой лишь наӯстолько, чтобы были возбуждены в основном не слишком высоӯкие колебательные уровни. Тогда колебания являются малыми (а потому и гармоническими), и уровни энергии определяются обычным выражением ħw(u + 1/2).
Число колебательных степеней свободы определяет число так называемых нормальных колебаний молекулы, каждому из которых соответӯствует своя частота wa (индекс a нумерует нормальные колебаӯния). Надо иметь в виду, что некоторые из частот wa могут совпадать друг с другом; в таких случаях говорят о кратной частоте.
Вычисление колебательной статистической суммы Zкол производится элементарно. Вследствие очень быстрой сходимости ряда суммирование можно формально распространить до u=¥. Условимся отсчитывать энергию молекулы от наиболее низкого (u = 0) колебательного уровня, т. е. включаем ħw/2 в постоянӯную e0 в
![]()
В гармоническом приближении, когда мы считаем колебания малыми все норӯмальные колебания независимы, и колебательная энергия есть сумма энергий каждого колебания в отдельности. Поэтому колеӯбательная статистическая сумма
![]() ,
,
распадается на произведение статистических сумм отдельных колебаний,

а для свободной энергии FKOJl получается сумма выражений
![]() ,
,
т. е.

В эту сумму каждая частота входит в числе раз, равном ее кратӯности. Такого же рода суммы получаются соответственно для колебательных частей других термодинамических величин.
Каждое из нормальных колебаний дает в своем классическом предельном случае (T>>ħwa) вклад в теплоемкость, равный c(a)кол = 1 при Т, большем наибольшего из ħwa , получилось бы скол = rкол . Фактически, однако, этот предел не достигается, так как многоӯатомные молекулы обычно распадаются при значительно более низких температурах.
Различные частоты wa многоатомной молекулы разбросаны обычно в очень широком интервале значений. По мере повышения температуры постепенно «включаются» в теплоемкость различные нормальные колебания. Это обстоятельство приводит к тому, что теплоемкость многоатомных газов в довольно широких интервалах температуры часто можно считать примерно постоянной.
Перейти на страницу: 1 2 3 4 5
